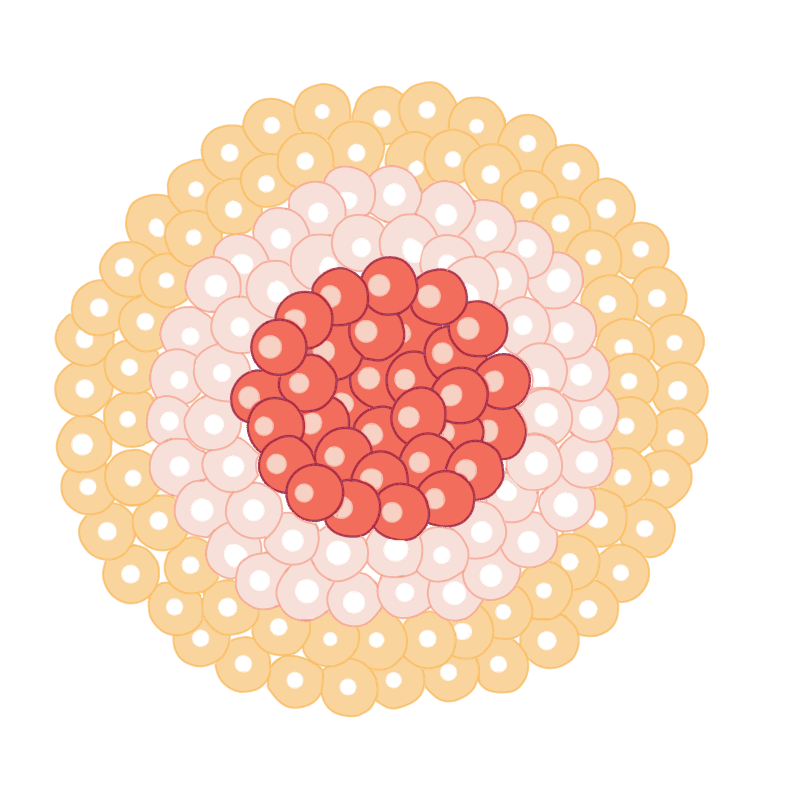
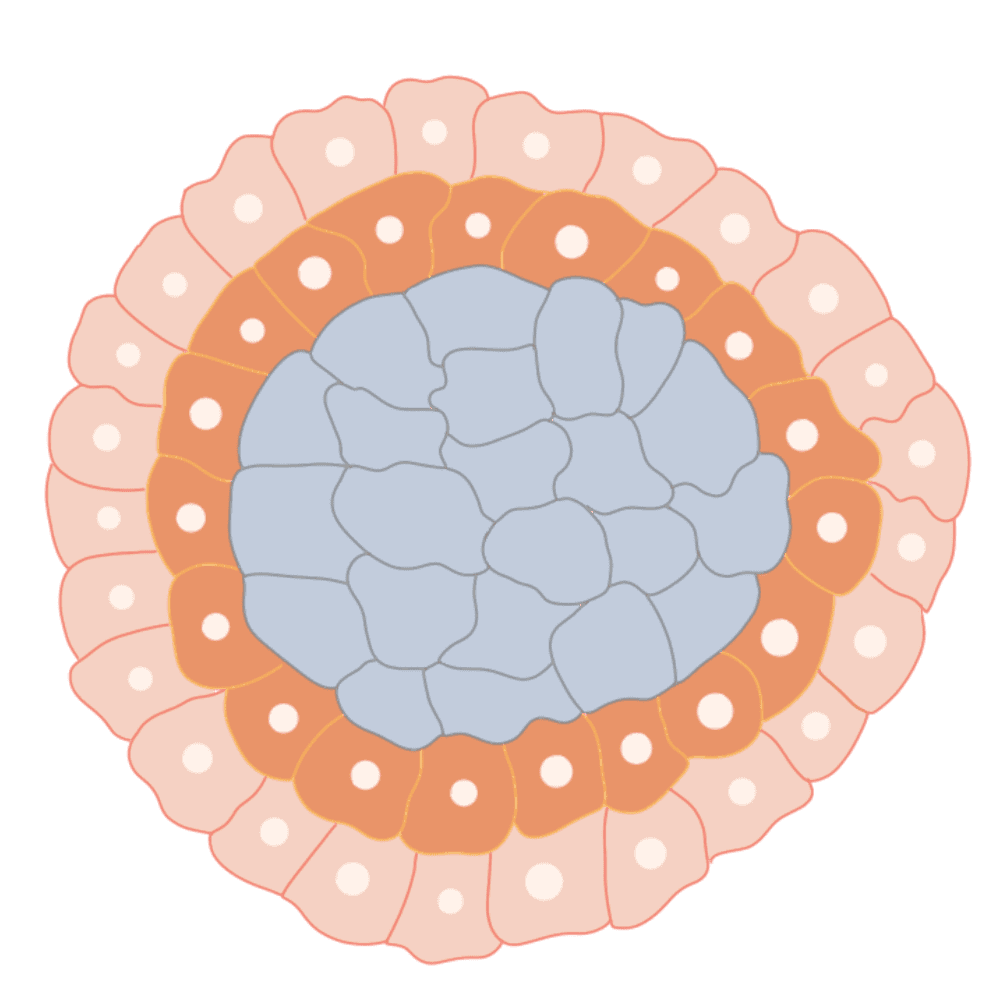
Viele In-vitro-Testsysteme und Ersatzmethoden zum Tierversuch basieren auf der Verwendung von Stammzellen. Als Stammzellen werden undifferenzierte Zelle eines vielzelligen Organismus verstanden, die in der Lage sind, unendlich viele weitere Zellen desselben Typs hervorzubringen und aus denen durch Differenzierung bestimmte andere Zelltypen entstehen können. Mithilfe von Stammzellen können Forscher:innen u. a. molekulare Mechanismen des Körpers und damit verbundene Krankheiten verstehen, patientenspezifische Krankheitsmodelle im Labor aufbauen und so bspw. durch die Testung von Wirkstoffen in diesen Modellen spezifische Therapieansätze entwickeln.
Embryonale und adulte Stammzellen
Embryonale (sogenannte pluripotente) Stammzellen können in alle Gewebe des Körpers differenzieren, während sich adulte (multipotente) Stammzellen nur noch in bestimmte Gewebetypen entwickeln können. Für die Forschung und die Medizin sind embryonale Stammzellen aufgrund ihres Differenzierungspotenzials zwar grundsätzlich besonders interessant, jedoch ist deren Verwendung und insbesondere Gewinnung ethisch höchst problematisch, da für deren Gewinnung ein menschlicher Embryo zerstört werden muss.
Die Verwendung adulter Stammzellen ist zwar ethisch weit weniger problematisch, jedoch können diese bereits spezialisierten Stammzellen nur noch bestimmte Zelltypen des menschlichen Körpers (z. B. verschiedene Zelltypen der Haut, nicht aber Blut- oder Nervenzellen) hervorbringen.
Induzierte pluripotente Stammzellen (iPS)
Ethisch weit weniger problematisch als die Arbeit mit embryonalen Stammzellen ist die Verwendung von sogenannten induzierten pluripotenten Stammzellen (iPS). Aufgrund ihrer Differenzierungseigenschaften sind iPS-Zellen fast genauso vielseitig wie embryonale Stammzellen. Durch eine künstliche Reprogrammierung von nicht-pluripotenten Körperzellen (sogenannten somatischen Zellen) kommt iPS-Zellen ein fast ebenso hohes medizinisches Potenzial zu als embryonalen Stammzellen. Medizinisch besonders interessant ist die Tatsache, dass bspw. aus einfachen Hautzellen eines/einer Patient:in patientenspezifische iPS-Zellen erzeugt werden können.